导言
2017 年 7 月 12 日,FDA 肿瘤药物专家咨询委员会(ODAC)以 10:0 全票推荐批准诺华 CAR-T疗法 Tisgenlecleucel (CTL-019)的上市。8月30日晚11时许,美国食药监局(FDA)官网发布消息称,他们做出历史性决定,批准了美国境内首款基因治疗方案、CAR-T治疗产品、诺华公司的CTL019,在美国上市。
据《华盛顿邮报》等媒体报道,诺华公司称,CTL019定价47.5万美元每位患者。这一价格使它成为最昂贵的癌症治疗产品之一。但如果患者在一个月的治疗后没有效果或响应,将不用支付治疗费用。
行业深度研究报告下载:乐晴智库网站 www.767stock.com
乐晴智库,行业深度研究(微信公众号:lqzk767)

这些结果意味着 CAR-T 疗法真正从临床试验阶段走向产业化阶段,我们通过 SWOT 分析对国内CAR-T 疗法产业化之路从临床治疗、生产流程、应用前景和审批监管四个维度进行深入分析,认为实现生产流程的标准化和规模化、有效规避安全性问题、具备专利先发优势以及合理的定价策略、符合国家审批监管政策的公司将会在国内 CAR-T 疗法产业化竞争中胜出。
本文完整报告请百度搜索“乐晴智库”获取。

CAR-T是一种肿瘤免疫细胞疗法
肿瘤免疫治疗是治疗癌症的新方法
传统的癌症治疗方法包括手术、放疗、化疗、靶向治疗,但这些传统的方法均具有不同程度的局限性,只能延缓并不能阻止病情的发展。手术治疗只适用于肉眼可见的肿瘤组织,放疗与化疗能杀死大量的肿瘤细胞,但由于其特异性不足,大量的正常组织细胞也会被破坏,产生很强的副作用。靶向药物由于肿瘤细胞的异质性和耐药性问题,幵不能发挥长期抗肿瘤功效。

肿瘤病人中,肿瘤细胞能规避免疫系统的识别和清除从而成功实现免疫逃逸,肿瘤免疫治疗是通过免疫学的原理和方法,提高机体免疫系统功能来抑制肿瘤生长、杀伤肿瘤,主要包括提高肿瘤细胞的免疫原性以及增强机体自身免疫细胞的肿瘤杀伤作用两大类。最近几年免疫治疗在黑色素瘤、非小细胞肺癌等肿瘤中的疗效逐渐获得肯定,甚至被医学界认为是肿瘤治疗领域中最具前景及最有可能治愈癌症的方向。

CAR-T 肿瘤免疫疗法的原理肿瘤免疫治疗包括非特异性刺激、免疫疫苗、免疫检查点单抗、过继细胞免疫治疗。其中过继性细胞治疗是指向肿瘤患者输注在体外培养扩增或者激活具有抗肿瘤活性的免疫细胞,通过增强机体抗肿瘤免疫能力来达到治疗肿瘤的目的。随着肿瘤免疫治疗的研究进展,细胞操作技术的迚步,过继性细胞治疗作为一种极具潜力的具有抗肿瘤活性的过继细胞免疫疗法,已成为研究热点。

CAR-T 是一种能够表达 CAR 的 T 细胞,全称是嵌合抗原受体 T 细胞免疫疗法。T 淋巴细胞在肿瘤的免疫应答中发挥重要作用,对肿瘤细胞具有极强的杀伤力。正常的 T 细胞发挥功能需要识别靶细胞表面的主要组织相容性复合物(MHC),肿瘤细胞能够降低表面 MHC 的表达从而逃脱 T 细胞的识别。

CAR(Chimeric Antigen Receptor)是嵌合抗原受体,能够以非 MHC 限制性方式识别肿瘤细胞表面的抗原。CAR 的组成是一个单链抗体(可特异性识别肿瘤细胞表面抗原),跨膜区(保证单链抗体在 T 细胞表面表达),共刺激信号片段(保证 CAR-T 细胞长期扩增活性,如 CD28 和 CD137),还有 T 细胞激活片段 CD3-ζ(保证信号传导激活 T 细胞)。
CAR 通过体外转染技术转到患者的 T 细胞内,使患者的 T 细胞表达 CAR 形成 CAR-T 细胞。经过改造后的 T 细胞能够非 MHC 依赖的特异性识别肿瘤表面相关抗原,同时保证处于激活扩增状态,长期对肿瘤细胞产生杀伤,从而达到抑制肿瘤生长、杀伤肿瘤的目的。

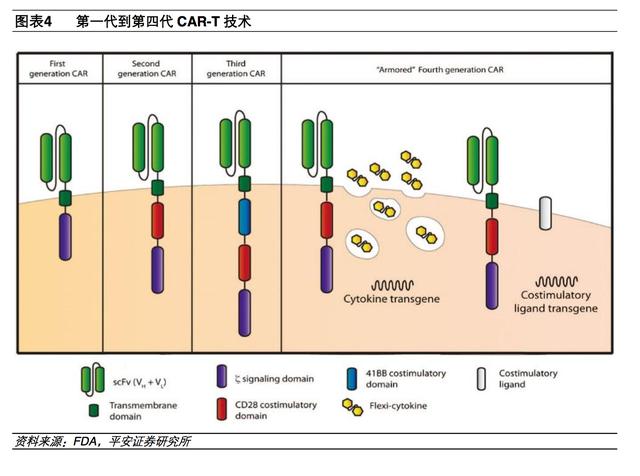
CAR-T 技术的研发进展CAR-T技术从产生至今已经有事十八年的历史,目前已经更新换代到了第四代。
(1)1989年以色列科学家研发出第一代CAR-T,第一代CAR没有共刺激信号片段,它没有解决 CAR-T细胞长期在体内存活的问题,导致它在临床没有什么疗效。
(2)第二代CAR成功的原因在于装上了第二信号通路的分子——来自抗原递呈细胞的共刺激信号的刺激。激活信号加上共刺激信号两条通路被激活,T细胞才有长期抗肿瘤的活性。
(3)第三代的CAR-T细胞有两个共刺激分子,为OX40和4-1BB,在体内试验显示出活性增强。然而两个共刺激分子引収T细胞活性的过度刺激可诱导细胞因子的分泌急剧增加。
(4)第四代CAR-T是在原有的CAR-T技术上加入自杀基因的可调控元件增加安全性与靶向性,或者加入外源IL-12的分泌刺激,以解除体内免疫抑制微环境。
CAR-T临床治疗SWOT分析
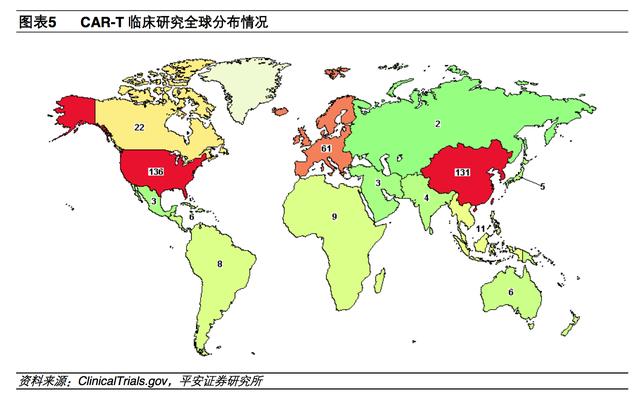
CAR-T 疗法从 2010 年开始进入临床,目前全球临床试验正如火如荼,美国在 CAR-T 临床实验上始终处于世界前列。
根据美国临床试验数据库(ClinicalTrails.gov)的数据,对于 CAR-T 细胞临床试验,截止 2017 年 7 月 31 日,美国以 136 项研究位列第一位,东亚地区则以 131 项排名第事(中国123 项、日本 5 项、中国台湾 2 项、韩国 1 项)。
2010 年时,全球所有的 CAR-T 临床试验都集中在美国,我国的 CAR-T 疗法临床试验是从 2013 年开始起步,2015 年中国注册的 CAR-T 临床数目占当年的新注册数目的一半,目前共有 123 项 CAR-T临床试验在进行中,数量上仅次于美国。虽然国内的 CAR-T 研究起步较晚,但是发展势头令人期待。
CAR-T 疗法主要的临床治疗流程:
1、预处理治疗:通常对病人迚行化学疗法预处理,减少体内的免疫抑制细胞(Tregs 和 MDSC),最常用的是美国国立卫生研究院(NIH)制定的氟达拉滨和环磷酰胺。
2、回输 CAR-T 治疗:将改造扩增好的 CAR-T 细胞回输到患者体内迚行治疗,需要严密监控患者的身体反应情况。
CAR-T 临床治疗的优势:个性化靶向治疗,对复发难治肿瘤疗效好
CAR-T 疗法是利用患者自身的 T 细胞进行改造回输,这就意味着每次治疗都是因人而异,需要做一套单独的 T 细胞改造生产方案,因此 CAR-T 疗法是一款定制疗法,每名患者的治疗方式都属于个体化治疗范畴。个体化治疗有助于提高疗效,减少不必要的毒副作用。
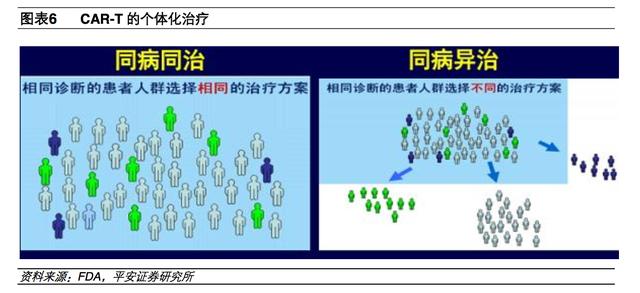
与此同时,由于对 T 细胞进行了 CAR 的转染改造,因此理论上来说 CAR-T 可以设定成任意靶点,具有高度靶向性,避免激活的 T 细胞对正常组织细胞造成伤害,因此 CAR-T 疗法也属于靶向治疗的范畴。
目前 CD19 是 CAR-T 疗法中最热门的靶点,CD19 是急性 B 淋巴细胞白血病(B-ALL)中肿瘤细胞表面普遍表达的抗原。自 2012 年以来,靶向 CD19 的 CAR-T 疗法在急性淋巴白血病患者的治疗中 取得了良好的治疗效果。目前三大 CAR-T 研収药企(诺华、Juno 和 Kite)在靶向 CD19 的 CAR-T在治疗白血病上均有较好疗效,同时三者竞争同样激烈。
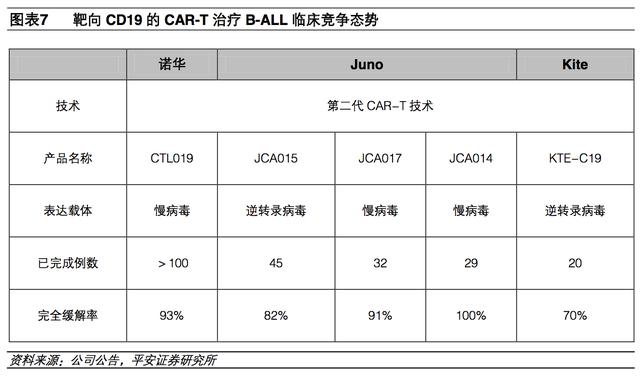
事代 CAR-T 技术能使 T 细胞表达促进自身增殖活化的基因,T 细胞进入体内后保持增殖分化能力,可以保证 T 细胞的长期存活,使患者具有长期的免疫功能,疗效更为持久。从已公布的临床数据来看,CAR-T 疗法的治疗效果令人满意。
获得更多数据分析及本文完整报告请百度搜索:乐晴智库

CAR-T 临床治疗的劣势:适应率低,竞争替代激烈
CAR-T 疗法属于靶向治疗,那么同样需要面对靶向药物的一大难题:适应症窄。CAR-T 疗法目前只针对特定靶点,只能用于该靶点表达异常的肿瘤,因此 CAR-T 疗法的适应症就比较窄。
美国是最早开启 CAR-T 疗法临床试验的国家,发展至今美国已经拥有最好的 CAR-T 产品和成熟的 CAR-T 临床治疗方案,针对的肿瘤类型也主要集中于白血病,骨髓瘤以及淋巴瘤。

此外,由于 CAR-T 疗法兴起后引起了众多生物医药企业的追捧,然而许多公司都将血液瘤作为主要适应症,这可能会造成对于特定疾病市场的供大于求,从长进角度来看,在 CAR-T 疗法商业化道路上有所建树的公司必须理性选择合适的适应症才能保持可持续发展。
CAR-T 疗法属于过继性细胞免疫治疗,在这一治疗范畴内还包括淋巴因子激活的杀伤细胞(LAK)、树突状细胞(DC)、细胞因子诱导的杀伤细胞(CIK)、肿瘤浸润淋巴细胞(TILs)、自然杀伤细胞(NK)、细胞毒性 T 淋巴细胞(CTL)和基因修改 T 细胞受体(TCR)等。经过数十年的研究,虽然 LAK、DC、CIK 等已被证实效果有限,但是 CAR-T、TCR-T、TILs 和 CAR-NK 等均有望成为突破性的治疗手段。因此,竞争替代可能会是 CAR-T 疗法临床治疗上所面临的最大挑战。
CAR-T 临床治疗的机会:靶点的多样化
基于 CAR 的基因重组改造促进了 CAR-T 技术的发展,通过增加 CAR 的表达元件从而增强 CAR-T的功能和安全性。未来随着 CAR-T 开发研究的深入,对 T 细胞的遗传改造不仅仅局限于通过 CAR的表达重塑其特异性,还可以通过引入其它靶点塑造 T 细胞新的靶向性和功能性。由于 CAR-T 细胞的识别杀伤过程不依赖 MHC,因此在选择适应症时只需要考虑靶点的特异性。目前,已有许多全新的靶点被引入 CAR-T 技术中包括 EGFR、HER2 和 PD1 靶点等,这些靶点为 CAR-T 疗法开发出更多的适应症奠定了基础。
CAR-T 临床治疗的挑战:解决大规模临床安全性问题
虽然目前 CAR-T 疗法的治疗效果很好,但其安全性问题也很突出。在临床试验中,不少病例都出现了细胞因子释放综合症(CRS),临床表现为发热、低血压等,同时还会出现神经系统毒性(头痛、抽搐、精神状态异常等)。这些症状一般在 CAR-T 细胞回输 24 小时左右开始出现,可以持续数天,严重的可能危及生命。
由于 CAR-T 疗法的不良反应具有致死性,目前各大公司对这些不良反应的应对有一定的经验积累,包括针对性的单抗药物,重症监护处理(ICU)等,都有效降低了不良反应的致死率。

如果 CAR-T 疗法进入大规模临床治疗阶段,能将安全性问题彻底解决,那么将是 CAR-T 疗法实现产业化的一个重要里程碑。鉴于此,FDA 也有意建立一个与 CAR-T 疗法的安全性相关的数据库,显示出 FDA 对 CAR-T 疗法安全性的关注。
目前已有不少公司利用四代 CAR-T 技术从源头上彻底解决 CAR-T 疗法的安全性问题。Juno 开发出一种双功能 CAR,在正常的 CAR 的基础上引入一个抑制性的 CAR,会识别正常细胞上面的另外一个抗原靶点,遇到正常细胞的时候,正常细胞上的另一个抗原会把 CAR 抑制住,通过这个方法来解决安全性问题。
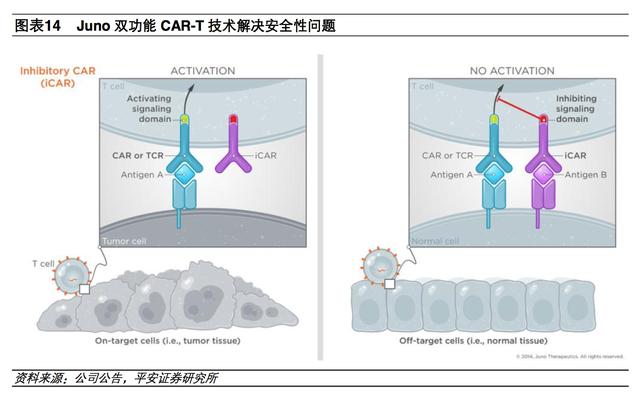 、
、
CAR-T生产流程SWOT分析
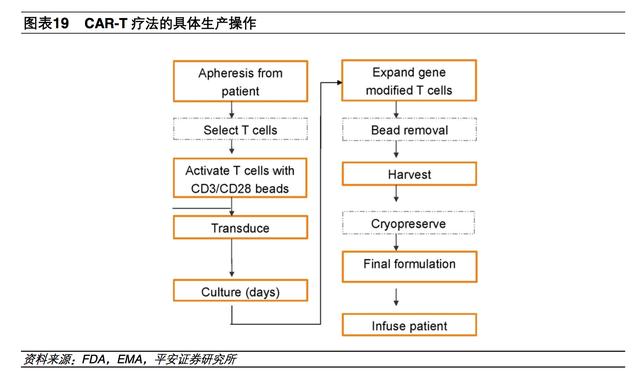
不同于实验室研究,在实际生产中,CAR-T 细胞治疗技术变得更加具体化,过程也呈现出较长的周期与高复杂度。CAR-T 生产流程从拿到供体的血液开始,经过 T 细胞分离幵转染形成 CAR-T 细胞,通过进一步扩增幵最终回输到病人体内,整个过程大约需要两周的时间。
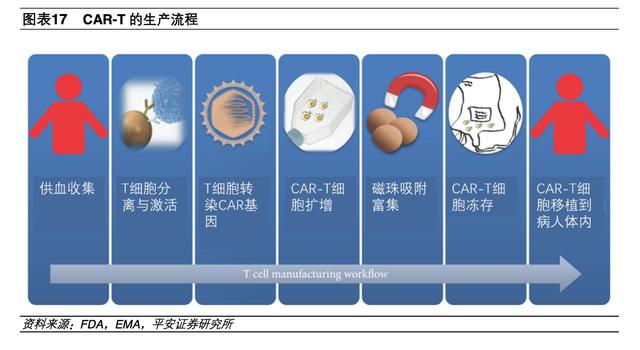
CAR-T 疗法的主要生产流程,分为 4 个步骤:
1、分离:从癌症患者身上获取血液,迚行分离提取获得 T 细胞。(需要确保 T 细胞的纯度)
2、改造:把通过基因工程技术改造的 CAR 转染迚入 T 细胞形成具有靶向性的 CAR-T。(需要确保病毒载体的安全性)
3、扩增:将 CAR-T 细胞迚行培养扩增,细胞量至少在十亿数量级。(需要追踪 T 细胞的状态和种类)
4、回输:将扩增好的 CAR-T 细胞迚行纯化富集后回输到病人体内。(需要确保 T 细胞的纯度和状态)
从 CAR-T 疗法的生产流程来看,影响 CAR-T 细胞质量的因素很多。不同的 CAR 受体,表达水平的不同,细胞生产工艺的各个环节差异等等因素都将会使得 CAR-T 疗法在治疗肿瘤的效果上产生差异。

CAR-T 生产流程的优势:技术壁垒高
CAR-T 疗法的生产研究基础是一个规范化、高效率以及高水平的 GMP 细胞生产中心,GMP 细胞生产中心的建立不仅需要资金和产地,还需要相关的工作和管理人员。由于 CAR-T 疗法的生产流程复杂,GMP 细胞生产中心的仪器设备、质量控制和人员操作等方面都需要有很高的要求,技术壁垒高,一般制药企业没有能力建立高水平的 GMP 细胞生产中心,因此无法迚入 CAR-T 细胞治疗领域进行竞争。
CAR-T应用前景SWOT分析
目前CAR-T疗法主要的应用集中于血液瘤领域。从临床适应症来看,CAR-T产品中迚展最快的CTL019(诺华)适应症为儿童和青少年复发难治性急性淋巴细胞白血病(ALL),紧随其后的是axicabtagene ciloleucel(Kite Pharma)适应症为弥漫性大B细胞淋巴瘤/ 原収性纵隔B细胞淋巴瘤/转化的滤泡性淋巴瘤,而JCAR017(Juno)的适应症为复収或难治性的侵袭性大B细胞非霍奇金淋巴瘤。从临床疗效来看,这三个产品的客观反应率都能达到80%,对于复发难治肿瘤而言非常令人满意。
此外在CAR-T产品的定价方面,诺华最近给出了47.5万美元的高昂定价范围,这是参照美国骨髓移植的费用而制定的价格。未来随着技术的发展和竞争产品的上市,CAR-T产品的价格会不断下降。


CAR-T SWOT分析结论
临床治疗 SWOT 分析结论,安全性问题是 CAR-T 临床治疗的关键:CAR-T 优势是个性化靶向治疗,对复发难治肿瘤疗效好;劣势是适应率低,竞争替代激烈;机会是靶点的多样化;挑战是解决大规模临床安全性问题;
生产流程 SWOT 分析结论,标准化和规模化在 CAR-T 生产过程中缺一不可:CAR-T 优势是技术壁垒高,规避竞争;劣势是生产过程繁琐,生产制备周期长;机会是生产的标准化和模块化;挑战是生产工艺的质量控制;
应用前景 SWOT 分析结论,专利是 CAR-T 应用的保障,定价是 CAR-T应用的关键:CAR-T 优势是在血液瘤适应症上的市场空间巨大;劣势是疗法价格昂贵;机会是在实体瘤中的疗效突破;挑战是 CAR-T 的专利保护和价格策略;

审批监管 SWOT 分析结论,细胞治疗政策完善有利于产业化进程:CAR-T优势是国家积极支持细胞治疗的临床应用;劣势是国内对疗法审批缺乏经验,没有先例;机会是国内可以学习美国细胞治疗的分层监管模式;挑战是细胞治疗相关政策的不确定性和不连续性。
我们认为实现生产流程的标准化和规模化、有效规避安全性问题、具备专利先发优势以及合理的定价策略、符合国家审批监管政策的公司将会在国内 CAR-T 产业化竞争中胜出 。
深度行业研究报告下载:乐晴智库网站 www.767stock.com
乐晴智库,行业深度研究
微信公众号:lqzk767
个人微信号:lqzk777
新浪微博:乐晴智库

4000520066 欢迎批评指正
All Rights Reserved 新浪公司 版权所有

