每年,全球数百万儿童需要接受手术麻醉,虽然单次麻醉相对安全,但3岁以下儿童接受多次麻醉或长时间麻醉,会导致包括认知功能下降、执行功能障碍和运动协调障碍等在内的长期神经功能障碍。因此,新生期麻醉毒性被美国FDA明确警示。
值得注意的是,上述长期神经功能障碍均与少突胶质细胞所形成的髓鞘功能密切相关。因此,近年来少量研究探讨了少突胶质细胞在新生期麻醉毒性中的关键作用,提示包括异氟醚、七氟醚和丙泊酚在内的全麻药物都会导致少突胶质细胞死亡,促进髓鞘形成可显著改善麻醉后的长期神经功能缺陷。然而,髓鞘具有高度可塑性,其形成可持续至成年,为什么全麻药物的神经毒性却仅发生在新生期之前呢?
近日,空军军医大学西京医院麻醉与围术期医学科、教育部麻醉学重点实验室刘慧青(第一作者)、苏斌虓(第一作者)、钟海星(通讯作者)、董海龙(通讯作者)等人在Journal of Advanced Research(IF=11.4)发表了题为“Neonatal sevoflurane exposures inhibits DHHC5-mediated palmitoylation of TfR1 in oligodendrocytes, leading to hypomyelination and neurological impairments”的研究,发现多次七氟醚暴露可显著增加少突胶质细胞内转铁蛋白受体TfR1的内吞,导致胞内铁超载和铁死亡发生,而TfR1仅于P21前的新生期表达。进而,单细胞测序筛选到棕榈酰化酶DHHC5下调,是促进TfR1内吞的关键;确认了少突胶质细胞DHHC5通过TfR1诱导前额叶皮质、海马和胼胝体区少突胶质细胞和神经元的铁死亡,最终导致长期神经功能障碍。

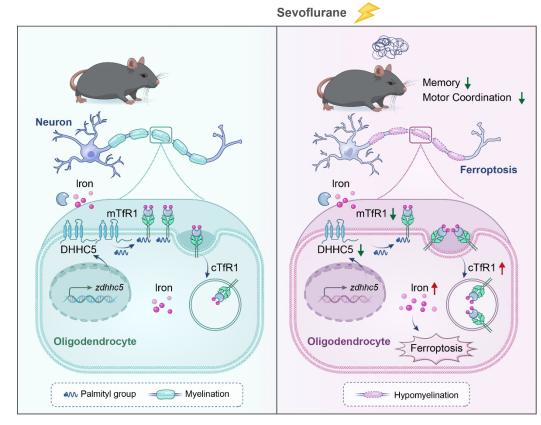
研究者发现,新生期(P6-8)七氟醚多次暴露可导致青春期胼胝体超过1700个基因改变,尤其是铁代谢相关通路的异常(图1)。一般认为,新生期少突胶质细胞内铁离子水平超过神经元6倍,是启动髓鞘发生的重要辅酶。而该研究证实,七氟醚多次暴露会导致小鼠胼胝体少突胶质细胞铁离子水平增加与铁死亡发生,持续至青春期。应用特异性铁死亡抑制剂Fer-1不仅逆转了铁死亡,更可恢复青春期胼胝体的髓鞘厚度,改善长期记忆缺陷和运动协调能力,提示少突胶质细胞铁死亡是新生期麻醉毒性的关键原因。
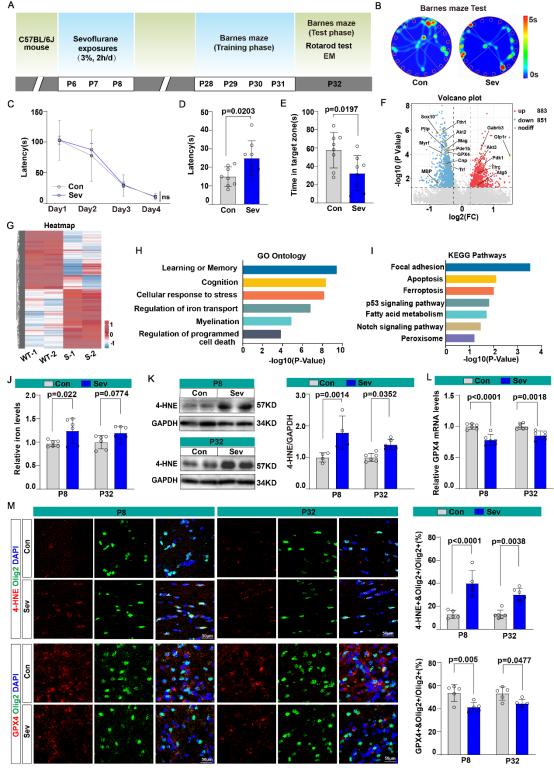 图1 新生期七氟醚多次暴露导致青春期铁代谢异常和髓鞘变薄
图1 新生期七氟醚多次暴露导致青春期铁代谢异常和髓鞘变薄进而,筛选到新生期多次麻醉暴露后TfR1基因表达上调,虽然总蛋白水平不变,但其内吞在青春期显著增加,这可能与棕榈酰化修饰减少有关。有趣的是,TfR1仅在在少突胶质细胞P21前短暂高表达,与新生期麻醉毒性的时间窗高度吻合。结合单细胞测序,研究筛选到了关键棕榈酰化酶DHHC5,明确了DHHC5通过对TfR1蛋白C98位点进行棕榈酰化修饰,促进少突胶质细胞成熟,减少其铁死亡(图2)。最后,使用转基因动物,研究验证了特异性上调少突胶质细胞中DHHC5表达,不仅可以抑制TfR1的内吞及其诱发的铁死亡,改善髓鞘发育;还可以显著抑制前额叶皮质,海马和胼胝体的神经元铁死亡,从而挽救青春期神经功能障碍(图3)。
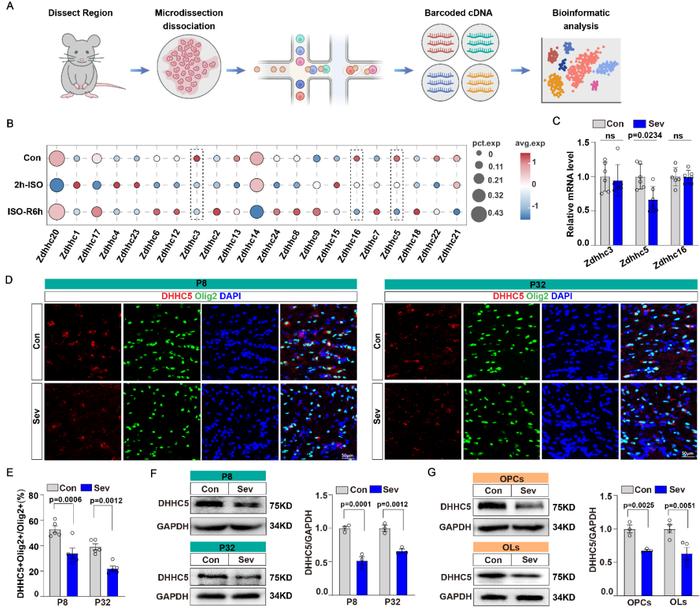
图2 DHHC5下调是TfR1棕榈酰化修饰减少的关键原因
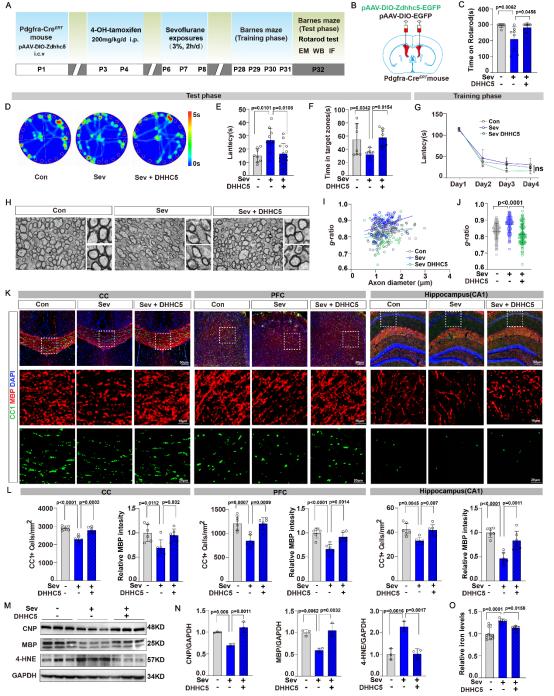 图3 特异性上调少突胶质细胞DHHC5改善新生期多次麻醉暴露引起的青春期髓鞘异常与神经功能障碍
图3 特异性上调少突胶质细胞DHHC5改善新生期多次麻醉暴露引起的青春期髓鞘异常与神经功能障碍综上所述,该研究首次揭示了新生期短暂表达的TfR1可能是介导麻醉毒性时间窗的关键分子,证实少突胶质细胞DHHC5介导的TfR1棕榈酰化是启动少突胶质细胞和神经元铁死亡并导致长期神经功能障碍的重要原因。上述结果不仅首次证实了少突胶质细胞与新生期多次麻醉暴露导致长期神经功能障碍间的因果关系,还为开发新的治疗策略提供了可能靶点。
本研究获得国家自然科学基金重点项目、陕西省自然科学基金“杰出青年基金”项目、广东省科技攻关计划项目等资助。


财经自媒体联盟

4000520066 欢迎批评指正
All Rights Reserved 新浪公司 版权所有

















































 第一财经日报
第一财经日报  每日经济新闻
每日经济新闻  贝壳财经视频
贝壳财经视频  尺度商业
尺度商业  财联社APP
财联社APP  量子位
量子位  财经网
财经网  华商韬略
华商韬略