6月10日,石药集团的股价飙升至近三年来最高点,市值再次突破千亿。
一方面,得益于近期中国创新药领域环境的积极变化,资本市场再次展现出浓厚的兴趣。
6月9日,中共中央办公厅、国务院办公厅印发《关于进一步保障和改善民生 着力解决群众急难愁盼的意见》提出,推进优质医疗卫生资源共享。特别提到,完善基本医疗保险药品目录调整机制,制定出台商业健康保险创新药品目录,更好满足人民群众多层次用药保障需求。
另一方面,石药集团此前公布的150亿美元三大BD中,已有项目成功落子。
6月6日,石药集团旗下新石生物向韩国LigaChem生物科学授予两项新型抗体的全球独家开发及商业化权利,用于针对肺癌、结直肠癌等实体瘤的抗体药物偶联物(ADC)研发。
千亿市值的背后,是中国创新药“出海”叙事的又一次高光时刻。而40%的退货率也暴露出中国创新药全球化进程中“信任危机”。
这场市值狂欢的背后,究竟是中国药企技术突破的实力印证,还是海外授权热潮下暗藏的风险预演?

01、50亿美元石药ADC授权再下一城
5月30日,石药集团就发布公告称,其正与若干独立第三方磋商三项潜在交易,涉及旗下表皮生长因子受体抗体药物偶联物(EGFR-ADC)等产品的开发、生产及商业化授权合作。每笔交易的潜在首付款、开发里程碑付款及商业化里程碑付款合计可达约50亿美元。其中一项交易已处于后期阶段,预计2025年6月完成。
石药股价与今年最低点飙升125%,旗下新诺威股价与今年最低点飙升188%(达上市以来最高点)。
虽然未公布具体信息,但根据交易金额来看,石药集团潜在授权的买家需拥有充沛的资金,可能为国际大型制药企业(如罗氏、阿斯利康、辉瑞等)。
如今,答案正式揭晓。6月6日,韩国LigaChem生物科学公司宣布已从NovaRock(“新石生物”)获得两项新型抗体的全球独家权利,以加速其针对难治性实体瘤的ADCs管线研发。
Novarock Biotherapeutics (“新石生物”)是石药集团香港控股公司旗下的Dragon Merit Holdings Limited投资和美国专家团队共同创立的生物大分子创新研发公司。
LigaChem生物科学是一家专注于抗体药物偶联物(ADC)研发的韩国生物科技公司,与药明合联、三星生物等全球CDMO企业合作加速临床转化。
根据协议,LigaChem公司将获得这两项新型抗体的全球独家开发和商业化ADC(抗体药物偶联物)的权利。出于保密考虑,交易的具体财务和技术细节并未公开。然而,该公司强调,其研发管线专注于解决那些尚未得到充分满足的癌症治疗需求。
据悉,新引入的两个靶点在多种实体瘤中表现出高表达性,涵盖了肺癌、结直肠癌、胃癌以及胰腺癌等。目前,针对这些特定靶点的ADC药物尚未有获批上市的产品。
LigaChem公司致力于运用NovaRock的差异化抗体技术,并与自身的ADC平台相结合,以加快候选药物的筛选进程和临床试验的准入。鉴于这些靶点的稀有性和显著的治疗潜力,该公司强调,这些候选药物将被战略性地定位,以寻求全球范围内的对外授权机会。
尽管未透露具体细节,但可以明确的是,交易聚焦于抗体偶联药物(ADC)领域。石药集团已经公开的处于临床阶段的ADC产品管线有近10款,这些产品针对HER2、EGFR、Claudin18.2等关键靶点。

其中,有三款已达成海外授权。业内有猜测,或许本次授权管线之一是石药未公开新靶点ADC。从在2025年美国癌症研究协会(AACR)年会上的趋势或可猜测靶点有可能是CDH17。
CDH17是近期ADC领域中备受瞩目的新兴靶点之一。根据表达谱分析,CDH17在超过50%的胃癌、90%至95%的结直肠癌、53%的胆管癌、50%的胰腺癌以及部分肝癌病例中均有表达。在2025 AACR上,12家制药企业集中展示了他们针对CDH17靶点的ADC药物研发的最新进展,其中中国药企扮演了主要角色;而石药并不在其列。
此外,石药集团此次的BD利好消息并非没有争议。
02、40%退货率敲响警钟买家巨额支出后更谨慎
从创新药对外授权交易的规模和活跃度来看,中国已成为全球最大的卖方市场。
而据不完全统计,截至2025年4月,在2020年完成的中国药企License-out交易中,“退货率”已高达40%。此外,有多个项目在今年宣布终止合作,其中就包括石药集团的ADC项目。
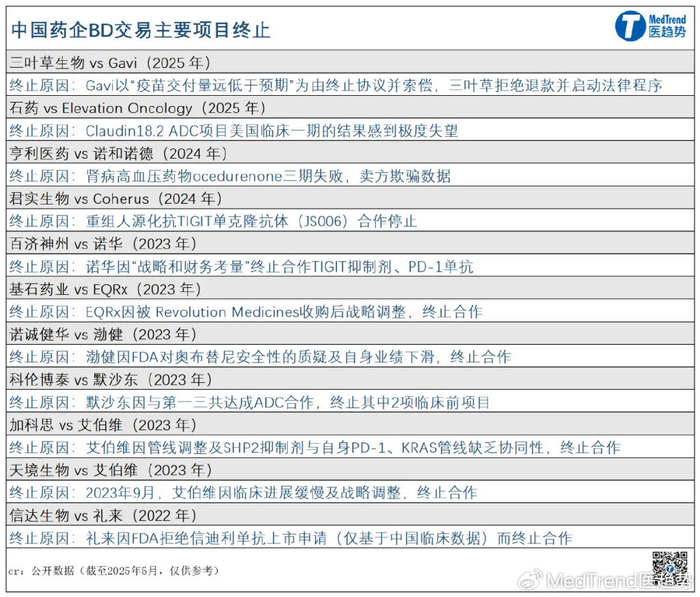
3月20日,Elevation Oncology宣布,终止从石药引进的Claudin18.2 ADC项目EO-3021/SYSA1801。
该项目在2022年7月由Elevation从石药集团引进,但不到三年的时间便被退回。Elevation Oncology在声明中措辞犀利,表示“对美国临床一期的结果感到极度失望(deeply disappointed)”。他们认为与其他Claudin18.2 ADC相比,该项目未能展现出足够的竞争力,且“未能达到我们的成功标准,也无法为患者提供有竞争力的收益风险比。”
而今年另一项“重磅退货”事件来自诺和诺德与亨利医药,并闹上法庭。2月14日法院作出裁决,亨利医药及其创始人兼执行董事长黄振华博士需向诺和诺德赔偿8.3亿美元(约60亿元)。
2023年10月,诺和诺德以13亿美元的总价引进了KBP Biosciences的肾病高血压药物ocedurenone。2024下半年,在一项针对慢性肾病的3期试验中,该药物未能改善收缩压,诺和诺德因此放弃了这一资产。
诺和诺德指控KBP公司隐瞒了药物(奥西度瑞酮,ocedurenone)的2期试验数据,这些数据显示该药物无效。
新加坡法院表示,可认为KBP故意未披露关键信息,包括显示ocedurenone无效的2期临床试验中期分析结果,以及关于单个产生异常阳性结果的测试点的质量和合规性问题的信息。同样,KBP的创始人、执行董事长黄博士可能也知情并参与了这些误导性陈述。
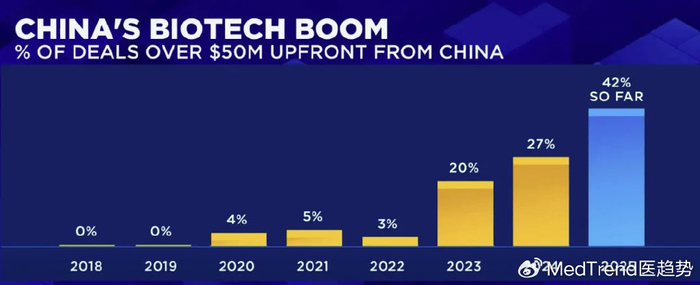
从中国创新药对外授权交易金额屡创新高来看,行业正经历从技术积累的初期阶段向全球价值实现的成熟阶段的飞跃。截至2025年,交易额超过5000万美元的中国创新药重大交易占比已达到42%。
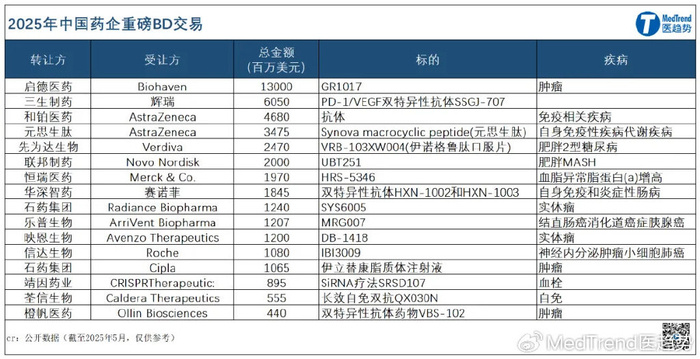
2025年Q1,中国创新药BD交易总金额同比增加超过200%,其中超10亿美元的达11笔,占全球近半。
比如,5月20日,三生制药PD-1/VEGF双抗(SSGJ-707)以12.5亿美元首付款授权辉瑞,刷新中国双抗“出海”单笔交易金额新纪录。
而随着交易金额的不断增加,买方公司所面临的风险也随之增大。
在本周一的高盛活动中,辉瑞公司首席执行官Albert Bourla表示,三生制药提交的数据给人留下了深刻印象,但是这些数据源自中国。基于此,辉瑞决定对三生制药进行深入研究,并在尽职调查过程中采取了“极其谨慎”的态度。辉瑞的尽职调查涉及多层级的参与,从Albert Bourla本人到中国实地团队。
Albert Bourla强调:“我们没有仅在数据室内进行尽职调查,而是派出了实地考察团队。我们派遣的团队前往中国,他们在那里停留了数周,访问了研究中心,仔细审查了试验结果,并与负责研究的医生进行了交谈,这让我们感到非常满意。我本人也与三生制药的首席执行官会面,他们是一个值得信赖的团队。”
同时,Albert Bourla指出,辉瑞只有在“整个项目取得巨大成功且销量极高”的情况下才会支付全部60亿美元。这一声明暗示了部分付款与重大销售里程碑相关联,即便如此,这笔交易已经是针对单一在研资产的巨额投资。
辉瑞将SSGJ-707视为战略资产,因为它有望取代PD-1/L1免疫检查点抑制剂,并与公司的抗体偶联药物(ADC)组合产生协同效应。该组合的核心资产源自辉瑞对Seagen的收购,包括以维汀(vedotin)为载荷的ADC药物。基于维汀的Pacdev与K药已被证实具有良好的协同效应,其对SSGJ-707与维汀类ADC的完美搭配持乐观态度。

4001102288 欢迎批评指正
All Rights Reserved 新浪公司 版权所有

