1.什么是类器官?(Organoids)
类器官(Organoids)指利用成体干细胞或多能干细胞进行体外三维(3D)培养而形成的多细胞团,具有自我更新(self-renewal)和自我组织(self-organization)能力,并且维持了其来源组织或器官的生理结构和功能的特点。类器官在各大研究领域显示出强大的潜力,包括再生医学、精准医疗以及药物毒性和药效试验、细胞疗法、器官移植等方面。
目前构建类器官的细胞主要来自胚胎干细胞(ESC)和诱导多能干细胞(iPSC)。胚胎干细胞从囊胚期的内细胞团分离,获取的数量非常有限,同时涉及伦理问题。而诱导多能干细胞(iPSC)是通过导入特定的转录因子将终末分化的体细胞重新编程为多能性干细胞,具有早期胚胎干细胞的发育能力,可分化成任何成体细胞与器官类型。基于这些显著的优势,iPSC已成为培育类器官重要的细胞来源。
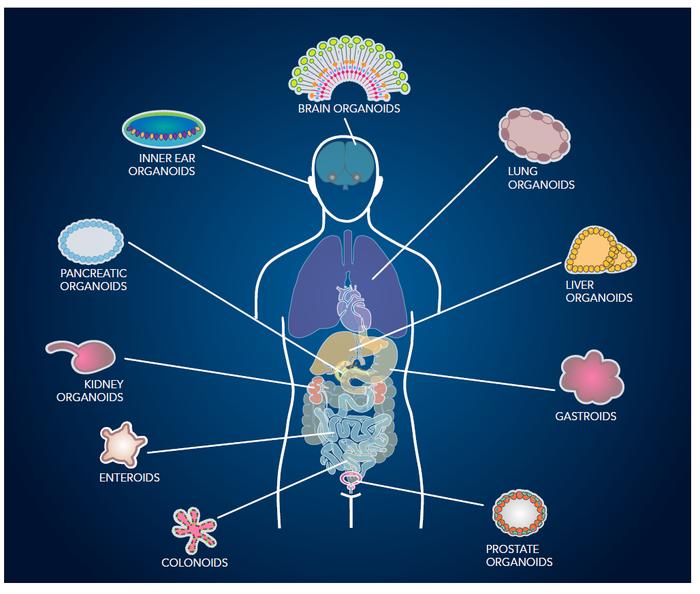
2. iPSC来源类器官的重大突破
iPSC来源的迷你型肝脏
2013年,Takanori Takebe博士团队培养出首个利用iPSC制成的类器官“迷你肝脏”,不足的是,尽管他们能够建造并将其移植到患者体内,但该器官无法充分发挥功能,也无法长时间工作。2019年10月,该团队成功利用iPSC同时培育出了三种互相连接的类器官,包括肝脏、胰腺和胆管,这是首次利用iPSC成功培养出多种器官的研究,研究结果发表在2019年的Nature杂志上。
2020年6月,匹兹堡大学医学院的研究人员利用人皮肤细胞诱导成iPSC,构建了功能完备的微型肝脏,移植到大鼠中存活了四天。该肝脏类器官就像正常肝脏一样,会分泌胆汁酸和尿素。

iPSC来源的皮肤类器官
2020年6月,在Nature上发表的一篇研究论文中,来自美国波士顿儿童医院的科研团队利用人iPSC培养出皮肤类器官,4-5个月的时间中,不但形成了皮肤特有的多层组织,更包含了毛囊、皮脂腺和神经回路,接近完整的真实皮肤。

iPSC来源的心脏类器官模型
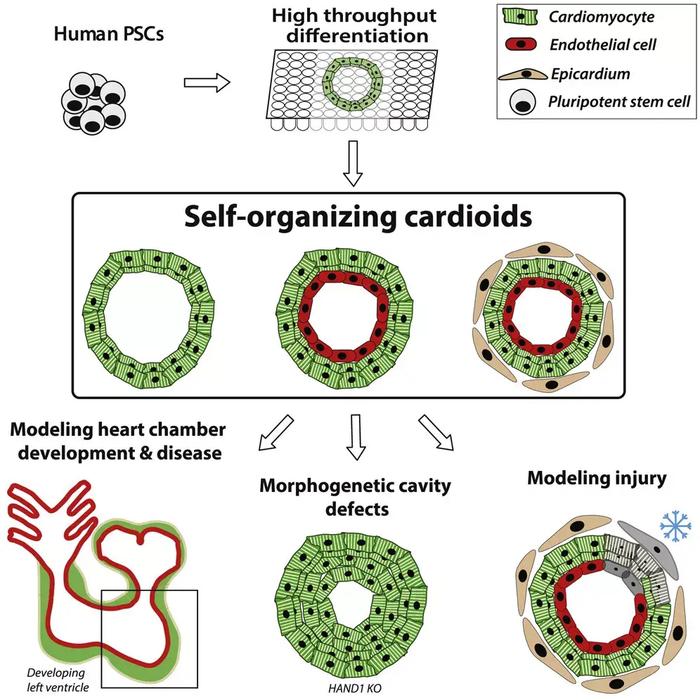
2021年5月,来自维也纳奥地利科学院的科研团队,使用人类多能干细胞成功培养出全球首个体外自组织心脏类器官模型,该模型可自发形成空腔,自主跳动,无需支架支持。同时,这种心脏类器官在受伤后可以自主动员心脏成纤维细胞迁移修复损伤。
目前,这一研究仅生成了一个单腔的心脏类器官结构,下一步,该团队计划在体外合成具有多个腔室的心脏类器官,就像人类真实的心脏那样。一旦这种多腔室自组织心脏类器官形成,人们就可以了解先天性心脏病的病因。
iPSC来源的视网膜类器官模型
2021年1月,来自美国国立眼科研究所(NEI)的科学家团队,采用患者iPSC构建了显性CRX-LCA的视网膜类器官模型,并利用该模型证明了使用腺相关病毒(AAV)载体递送CRX作为基因增强策略的可行性。该研究发表在Stem Cell Report期刊上,为开发治疗显性CRX-LCA和其他CRX视网膜病变的基因疗法提供了概念验证。

2021年4月28日,来自美国宾夕法尼亚大学的Guo-Li Ming教授及其团队在《Cell Stem Cell》上发表了题为“Generation of hypothalamic arcuate organoids from human induced pluripotent stem cells”的文章。该文章建立了一种从人诱导的多能干细胞中生成下丘脑弓状类器官的方法,该细胞表现出人弓状核的神经元亚型多样性和分子特征,可用于Prader-Willi综合征模型。

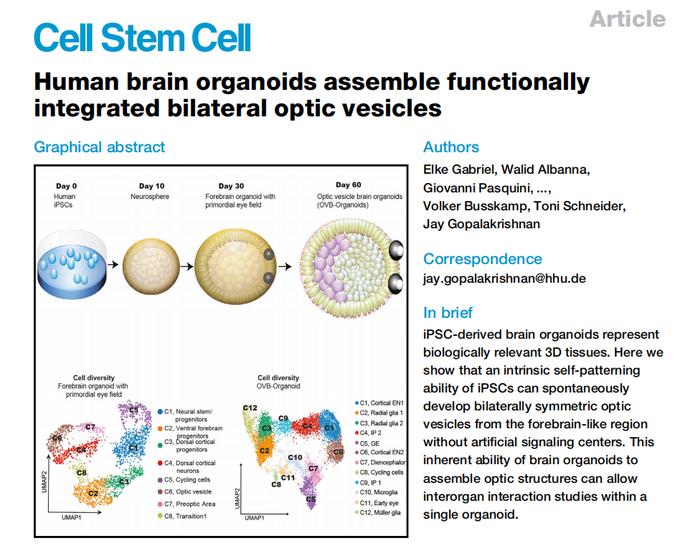
在一项最新的研究中,来自德国杜塞尔多夫大学等研究机构的研究人员发现iPSC可被用来构建含有一种叫做视杯(optic cup)的眼睛结构的大脑类器官模型。这种大脑类器官自发地从大脑类似区域的前部发育出双侧对称的视杯,包含不同类型的视网膜细胞,形成了能对光线作出反应的电活性神经元网络,也包含晶状体和角膜组织,并且视网膜与大脑相应区域相连。研究结果于2021年8月17日发表在Cell Stem Cell期刊上。
结语:
iPSC可以使用人体中所有类型的体细胞作为“原料”,来源十分广泛,同时具有早期胚胎干细胞的发育能力,在体外培养时通过构建合适的环境,模拟体内发育过程,理论上可分化成任何成体细胞。研究者们基于iPSC的突破性成果为类器官打开了一个全新的维度,近年来,衍生自诱导性多能干细胞的人脑类器官的发展,减少了研究活动中使用动物模型的试验,并为相关疾病的研究开辟了新视野。

4000520066 欢迎批评指正
All Rights Reserved 新浪公司 版权所有

