前言
心血管疾病 (CVD)仍然是西方国家死亡和发病的主要原因,因此需要有助于 CVD 发展和进展的新治疗靶点。非靶向代谢组学正在成为发现与疾病相关的途径的强大平台,作者对 T2DM 受试者的血浆进行了非靶向代谢组学分析,并结合机理研究,揭示了通过代谢途径形成的代谢物在 T2DM 受试者中增强,并与 T2DM 和非糖尿病受试者的 CVD 风险升高相关。
必需氨基酸苯丙氨酸(Phe)是肠道微生物群产生的代谢物苯乙酰谷氨酰胺 (PAGln)的营养前体,PAGln 在临床和机制上都与 CVD 相关,并显示通过宿主 G 蛋白偶联受体促进 CVD 相关表型,包括 α2A、α2B 和 β2-肾上腺素能受体 (ADR)。
本篇由美国克利夫兰诊所勒纳研究所心血管与代谢科学部Stanley L. Hazen教授课题组在Cell期刊(IF:66.850)发表了题为的研究成果,通过非靶向代谢组学、靶向代谢组学与肠道微生物菌群联合研究方法,发现了心血管疾病发生的特征,为心血管疾病防治提供了理论依据。
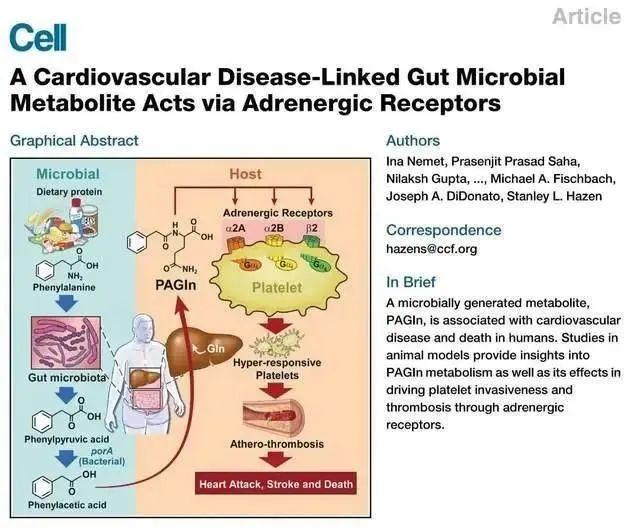
技术流程
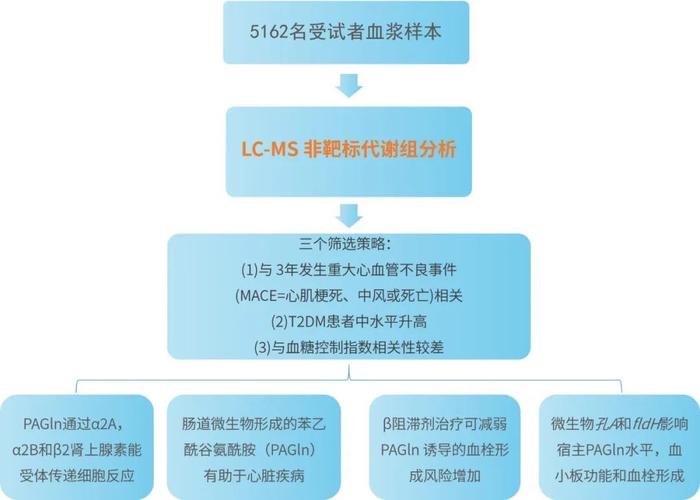
研究方法
研究材料/样本:
无菌小鼠,两个临床队列(5162名受试者)
主要组学研究方法:
LC-MS 非靶标代谢组分析、靶向代谢组学、肠道微生物研究
研究结果
1. 非靶向代谢组学:鉴定 PAGln 与 CVD 相关
对1162名受试者血浆进行非靶向代谢组学检测,三个筛选策略如下:(1)与事件(3年)主要不良心脏事件(MACE =心肌梗死(MI)、中风或死亡)相关;(2)T2DM水平升高;(3)与血糖控制指标的相关性差。研究发现一种与MACE最相关未知物(m/z 265.1188)满足筛选标准(图1A, B),经鉴定该物质为PAGln(图1C)。建立该物质同位素液相色谱串联质谱(LC/MS/MS)绝对定量方法,对另一独立队列(n=4,000,验证集)进行PAGln靶向验证,该队列中T2DM受试者和MACE受试者血浆PAGln水平都相对较高。Kaplan-Meier生存分析显示,高PAGln水平与MACE高风险显著相关(图1D),较高的PAGln水平仍是MACE风险的独立预测因子(图1E)。
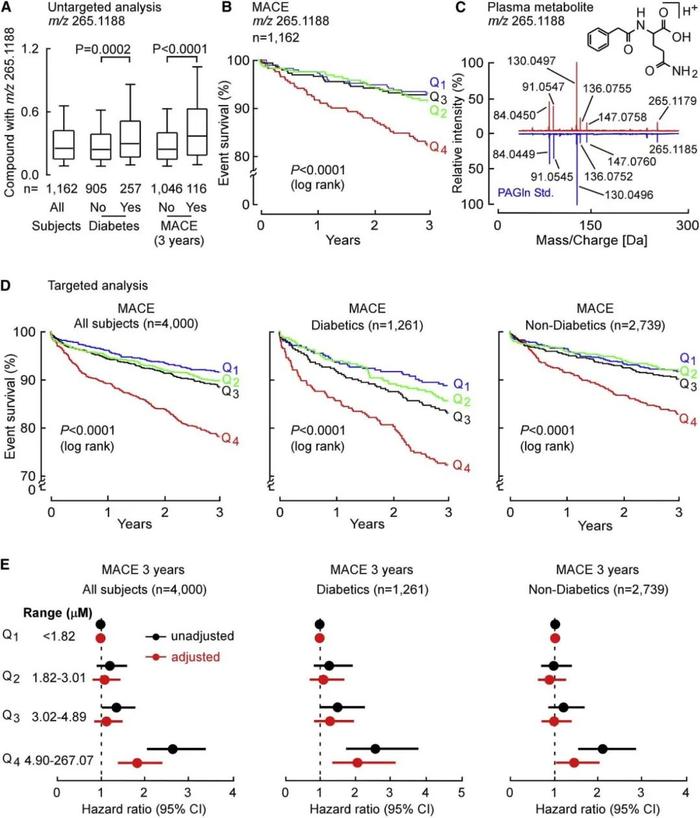
图1 | 非靶向代谢组学研究发现m/z为 265.1188 的代谢物与心血管疾病风险相关,随后被鉴定为苯乙酰谷氨酰胺
2. 功能验证:肠道微生物群参与体内PAGln 和苯乙酰甘氨酸的产生
通过检测基线(Pre-Abx)、7天广谱复合抗生素处理(Abx)和3周清除期菌群重塑(Post-Abx)的血浆PAGln水平(n=15),发现PAGln水平受肠道微生物影响(图2A)。有研究表明,PAGln由苯乙酸(PAA)与谷氨酰胺(Gln)在肝酶的作用下形成,而PAA由苯丙氨酸(Phe)经菌群代谢产生。此外,PAA也可与甘氨酸(Gly)结合形成苯乙酰甘氨酸(PAGly)。
研究人员评估了健康受试者(n=25)和小鼠体内PAGly及PAGln水平,结果发现,人体中以PAGln为主,而小鼠中以PAGly为主(图2B),小鼠腹腔注射PAA后,主要生成PAGly(图2C)。比较常规饲养和GF小鼠或Abx干预前后的血清PAGly水平,表明肠道菌群是生成PAGly的重要参与者(图2B, 2D)。因此,在人类和小鼠中,PAGln和PAGly都是通过一种代谢途径产生,饮食中的Phe通过肠道菌群转化为PAA,宿主与Gln(人类)或Gly(啮齿动物)发生共轭反应,分别产生PAGln和PAGly(图2E)。
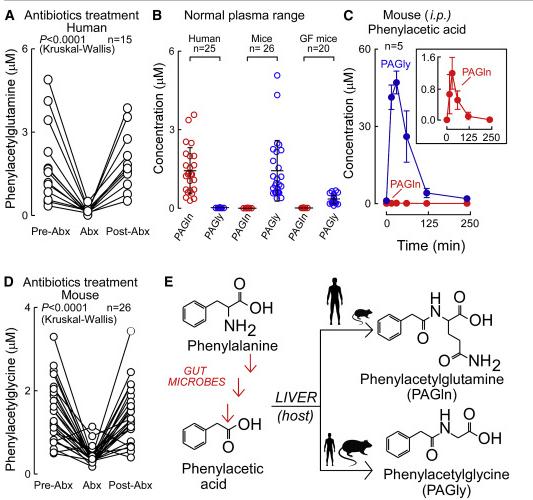
图2 | PAGln体内生产是人类和小鼠中微生物群依赖性的过程
3. 表型验证1:PAGln 增强血小板刺激诱导的钙释放和对多种激动剂的反应
根据人PAGln水平与血栓事件正相关性,提示PAGln可影响血小板功能和血管基质相互作用。研究结果显示,PAGln加速了胶原依赖性血小板粘附和扩散速度(图3A-3C),并呈现剂量依赖性(图3D, 3E),表明PAGln可能与血小板直接相互作用,促进胞质内Ca浓度([Ca]i)呈现依赖性升高,并进行了相关验证(图3G)。此外,在PAGly实验中也观察到类似结果。因此,肠道菌群相关代谢产物PAGln和PAGly显著影响血小板功能,增强血小板与胶原基质的粘附,以及血小板刺激依赖性[Ca]i升高和对激动剂的聚集反应。
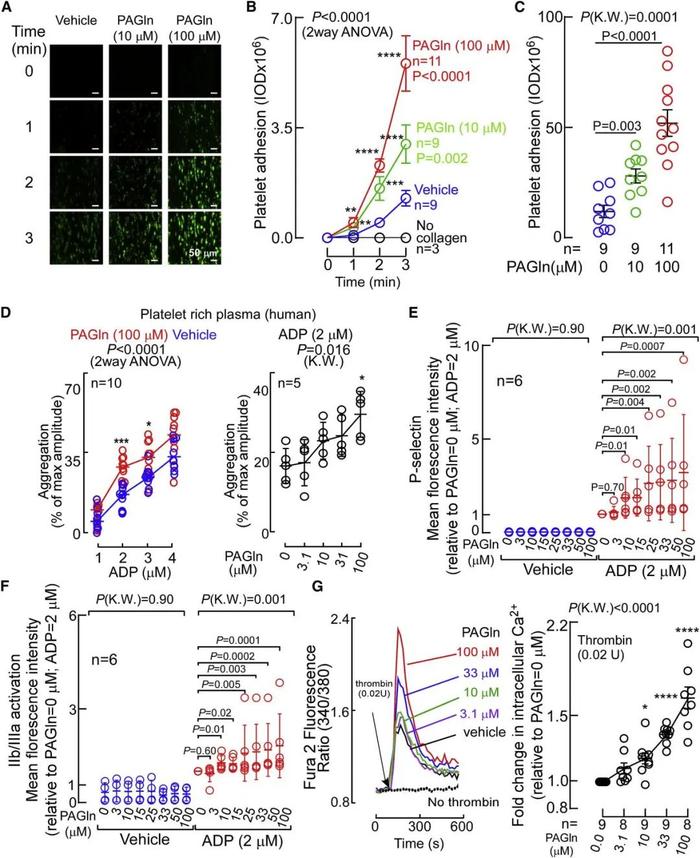
图3 | PAGln 增强血小板反应性
4. 表型验证2 :PAGln 加速血小板凝块形成并增强体内血栓形成潜力
通过FeCl诱导的颈动脉损伤模型研究发现,PAGln和PAGly都能加剧损伤的颈动脉内血栓形成(图4A),且与对照组相比,相应地减少了损伤后血流停止的时间(图4B)。
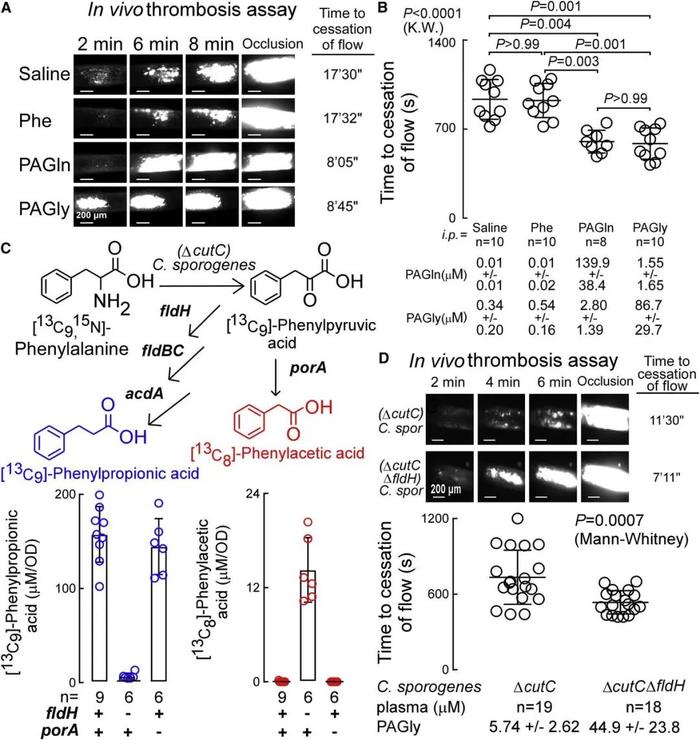
图4 | PAGln 和 PAGly 增强体内血栓形成的可能性
5. 机制探究1:肠道微生物基因porA和fldH在体内调节宿主血栓形成潜力
有研究报道Phe主要由生孢梭菌(Clostridium sporogenes)代谢为PAA(氧化途径)和苯丙酸(PPA)(还原途径),随后分别与Gln或Gly缩合形成PAGln或PAGly。其中参与反应的酶主要由porA或fldH基因编码。于是作者构建了porA或fldH基因缺失的C. sporogenes突变株。结果显示,含有功能性基因porA和fldH的(ΔcutC) C. sporogenes仅产生同位素标记的PPA,而不产生PAA;(ΔcutC,ΔfldH)C. sporogenes(具有porA功能)不再产生PPA;(ΔcutC,ΔporA)C. sporogenes(具有fldH功能)不再产生PAA(图4C)。然后通过突变株定植GF小鼠以及颈动脉损伤实验表明,基因porA主要影响PAA产生,而fldH主要调节PPA产生,且敲除fldH会增加PAA水平继而影响PAGly水平从而显著降低血栓形成。
6. 机制探究2:PAGln 通过 G 蛋白偶联受体介导细胞事件
研究发现,GPCR信号通路调节剂和抑制剂均显著降低了PAGln诱导的DMR反应(图5A,5B)。进一步研究发现PAGln可影响cAMP水平,并证实PAGln在多个细胞中包括分离出的人血小板中通过GPCR(s)介导细胞反应。研究人员发现PAGln与儿茶酚胺结构相似(图5E),暗示PAGln通过肾上腺素能受体(ADRs)发挥作用。遗传和药理学方法的功能丧失和功能获得研究证实,PAGln可通过G蛋白偶联受体(包括α2A,α2B和β2-ADRs)介导细胞反应(图5和图6A, B)。
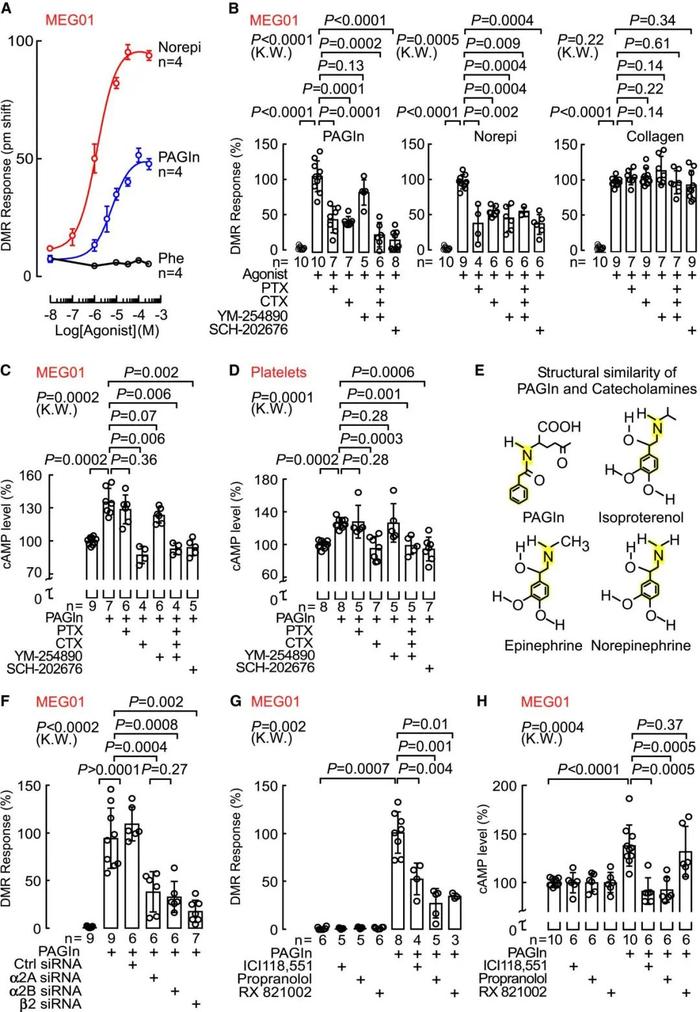
图5 | PAGln 通过 G 蛋白偶联受体和 ADR 介导细胞反应
7. 功能验证:肠道微生物群依赖性代谢物 PAGln 通过 ADR 发挥作用
通过功能增益研究证实 PAGln 可以通过 α2A、α2B 和 β2 ADR 发出信号,为了进一步证实 PAGln 通过 ADR 发挥作用的能力,研究者在人胚胎肾细胞(HEK293) 中单独过表达 α2A、α2B 和 β2 ADR 进行了功能获得性研究。在多种细胞类型中采用遗传或药理学方法的功能丧失和功能获得研究均证实 PAGln 可通过 α2A、α2B 和 β2 ADR 诱导细胞反应。
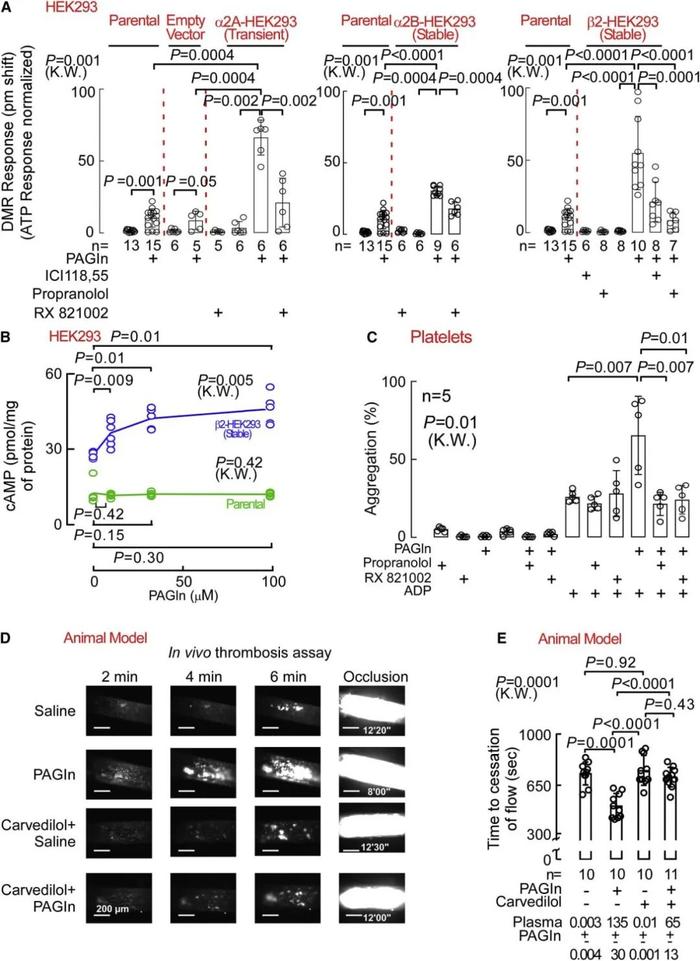
图6 | PAGln 通过 ADR 调节血小板功能和体内血栓形成潜力
研究讨论
目前的研究证实了肠道微生物群在人和小鼠的 PAGln(和 PAGly)生成中的主要作用,PAGln 升高与 CVD 风险之间的临床关联可能通过几种机制发生。首先,PAGln 可能通过多种互补方法影响血栓形成,其次,PAGln 可能与GPCRs (包括 ADRs)的相互作用影响 CVD 的相关表型。尽管目前的研究仅关注人类血小板中表达的三种 ADR,但可以推测 PAGln 具有调节其他 ADR 的潜力,因此可能会影响多种与 ADR 相关的体内生理过程。
研究证实,肠道微生物群衍生代谢物 PAGln 可增强全血、分离的血小板和动脉损伤动物模型中的血小板活化相关表型和血栓形成潜力。对人类共生体的功能和基因工程研究,再加上无菌小鼠的微生物定植,表明微生物基因有助于将膳食苯丙氨酸转化为 m/zporA苯乙酸,随后宿主产生 PAGln 和苯乙酰甘氨酸 (PAGly),促进血小板反应性和血栓形成潜力。使用遗传和药理学工具的功能增益和功能丧失研究均揭示 PAGln 通过 G 蛋白偶联受体介导细胞事件,包括 α2A、α2B 和 β2-肾上腺素能受体。因此,PAGln 代表了一种新的促进 CVD 的肠道微生物群依赖性代谢物,它通过肾上腺素能受体发出信号。
小鹿推荐
这项研究通过两个临床队列的非靶向代谢组学和靶向代谢组学以及微生物菌群的研究发现了一种新的心血管疾病相关的肠道菌群代谢衍生物——苯乙酰谷氨酰胺(PAGln),体内外实验揭示了该物质的菌群和宿主代谢途径,以及促进血栓形成的分子机制,证实了肠道菌群-代谢物在心血管等临床疾病中发挥着不容忽视的重要作用。为心血管疾病研究奠定了坚实的基础。
猜你还想看
1、中医药专题 | 北京协和药物所靳洪涛、贺玖明团队整合网络毒理学和质谱成像技术探究何首乌D组分肝毒性机制
2、Cell 新作|大豆中异黄酮可通过抑制血浆炎症标志物减轻引起的血管炎症
3、Cell新进展!人乳腺癌肿瘤及免疫生态系统的单细胞图谱
4、Nature | 肠脑轴:16S+代谢+转录揭示间歇性禁食改变肠道菌群,促进神经损伤修复
本文系鹿明生物原创
转载请注明本文转自鹿明生物

4000520066 欢迎批评指正
All Rights Reserved 新浪公司 版权所有

