慢性疼痛的发病率超过20% 1,严重影响生活质量。越来越多的研究表明,除神经元细胞外,非神经元细胞,特别是胶质细胞在疼痛的发病和缓解(resolution)中发挥着重要作用2。星形胶质细胞(astrocyte)在生理和病理条件下对中枢神经系统 (CNS) 发挥重要作用。值得注意的是,单个星形胶质细胞可以与啮齿动物大脑中大约 20,000-120,000 个突触相互作用,与人类大脑中大约 270,000 到 200 万个突触相互作用,凸显了它们对突触功能的重大影响。星形胶质细胞影响各种神经和神经精神疾病,包括阿尔茨海默病、帕金森病、多发性硬化症、慢性疼痛。因此寻找特异性的星形胶质细胞分子靶点,对疼痛等神经系统疾病的治疗具有重要作用。
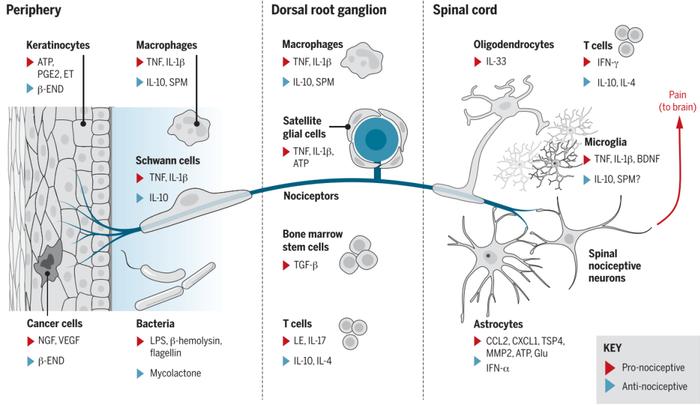
图1:伤害感受器与非神经元细胞之间的相互作用。Pain regulation by non-neuronal cells and inflammation.
Ji RR, et al. Science. 2016.
2025年2月13日,美国杜克大学Ru-Rong Ji教授团队在神经科学期刊Neuron杂志发表了题为:GPR37L1 identifies spinal cord astrocytes and protects neuropathic pain after nerve injury的研究论文。该研究鉴定了脊髓星形胶质细胞高度特异的G 蛋白偶联受体(GPCR)分子-GPR37L1,并且星形胶质细胞GPR37L1 通过谷氨酸转运蛋白-1 (GLT-1)调节脊髓背角的兴奋性突触传递,进而缓解神经损伤引起的神经性疼痛。此发现为慢性疼痛药物开发提供的新的靶点。

2019年,Ru- Rong Ji教授与University of Rochester Medical Center的Maiken Nedergaard教授在Nature Reviews Neuroscience杂志上发表综述文章3,总结了星形胶质细胞在慢性疼痛和慢性痒中的作用及其机制。本周Ru- Rong Ji教授教授团队在Neuron在线发布的研究论文进一步鉴定了新的对抗疼痛的星形胶质细胞细胞分子靶标。
首先,结合单细胞测序、原位杂交等方法,发现在GPCR家族中,Gpr37l1是脊髓背角星形胶质细胞最高表达并特异的GPCR基因之一。通过Gpr37l1基因敲除小鼠的疼痛行为学测试发现,Gpr37l1基因的缺失会加剧并延长小鼠的疼痛。
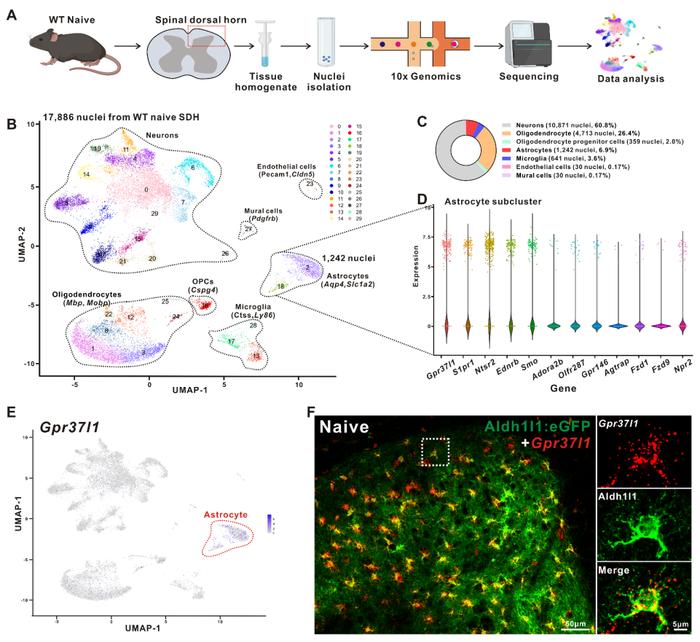 图2:单细胞测序和原位杂交鉴定Gpr37l1特异性高表达在脊髓星形胶质细胞。
图2:单细胞测序和原位杂交鉴定Gpr37l1特异性高表达在脊髓星形胶质细胞。进一步,在外周神经损伤模型SNI手术后,对脊髓胶质细胞的观察发现,Gpr37l1基因的缺失会加快星形胶质细胞的胶质化(astrogliosis)而不影响小胶质细胞的胶质化(microgliosis)。此结果证明了GPR37L1对脊髓背角星胶细胞在外周神经损伤后的形态起重要调控作用。
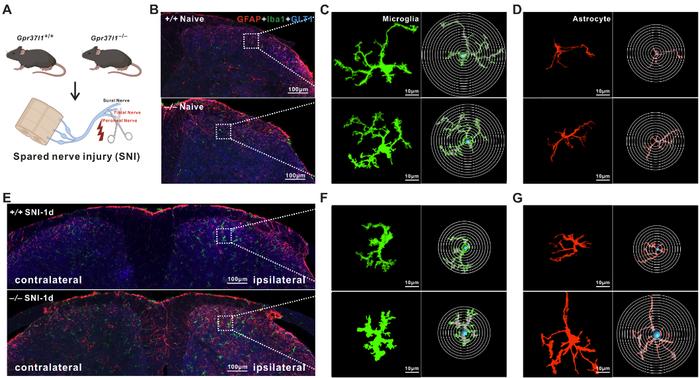 图3:Gpr37l1 缺乏并神经损伤在早期诱发脊髓背角星形胶质的胶质化。
图3:Gpr37l1 缺乏并神经损伤在早期诱发脊髓背角星形胶质的胶质化。除Gpr37l1基因敲除小鼠外,通过si-RNA以及AAV-sh:RNA敲低脊髓背角GPR37L1的表达后,发现引起了小鼠的痛行为表现,且增强了脊髓背角Vglut2阳性神经元的兴奋性突触传递(sEPSC)。进而通过Western Blot,proximity ligation assay,超分辨成像,AAV脊髓背角定点注射,脊髓片单细胞膜片钳纪律等方法,鉴定了星形胶质细胞GPR37L1通过GLT-1调节脊髓背角中的兴奋性突触传递。
最后,使用AAV-Gpr37l1:overexpression在脊髓定点注射过表达GPR37L1,及在Gpr37l1基因敲除小鼠上重新表达GPR37L1,发现可以预防和治疗神经病理性疼痛,抑制星形胶质细胞的胶质化而不影响小胶质细胞的胶质化,并抑制由外周神经损伤引起的脊髓背角兴奋性突触传递(sEPSC)的增强。值得注意的是,Ru-Rong Ji教授在2024年3月于Journal of Clinical Investigation杂志发表了Satellite glial GPR37L1 and its ligand maresin 1 regulate potassium channel signaling and pain homeostasis的研究论文4,发现外周神经系统,被根神经节(DRG)中的卫星胶质细胞(satellite glial cell)上特异性的表达GPR37L1,并鉴定药物maresin 1可以靶向星胶质细胞的GPR37L1治疗疼痛。本次发表于Neuron的文章同样发现maresin 1可以作用与脊髓背角星形胶质细胞GPR37L1,抑制脊髓背角谷氨酸神经元的兴奋性突触传递,并缓解疼痛。
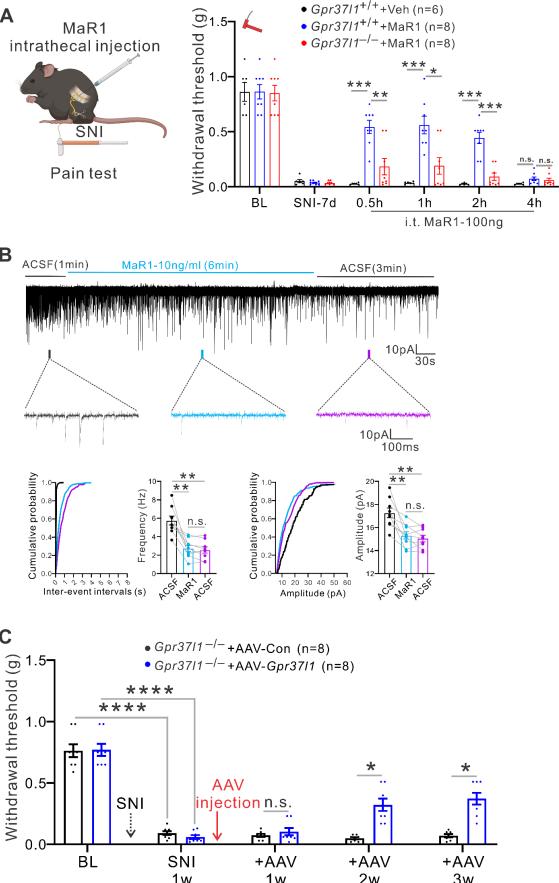 图4:Maresin 1或者脊髓背角过表达GPR37L1治疗神经病理性疼痛。
图4:Maresin 1或者脊髓背角过表达GPR37L1治疗神经病理性疼痛。神经系统的胶质细胞越来越收到研究人员的重视,通过新的技术手段,如单细胞测序,特异性基因敲低或过表达,高分辨率的光学成像等方法,人们进一步的探索胶质细胞的细胞生物学功能及其在神经系统中发挥的作用。本研究通过对GPCR家族的研究,鉴定了GPR37L1,这一孤儿GPCR在的星胶细胞中的作用,并提出了新的成药靶点。
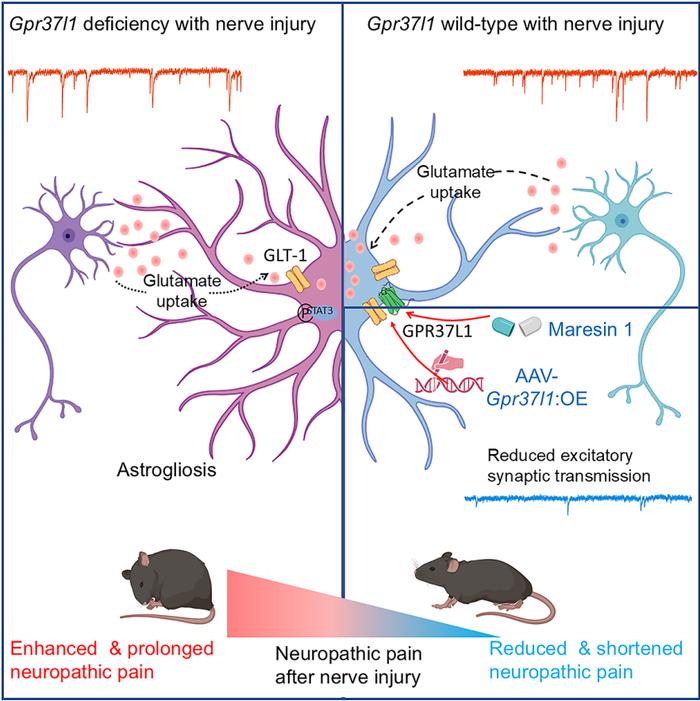 图5:脊髓背角星形胶质细胞GPR37L1 调控星形胶质细胞胶质化,突触传递和神经病理性疼痛。
图5:脊髓背角星形胶质细胞GPR37L1 调控星形胶质细胞胶质化,突触传递和神经病理性疼痛。杜克大学徐劲博士为论文第一作者。杜克大学杰出教授,麻醉学讲席教授,神经生物系教授,细胞生物系教授和疼痛研究中心主任的Ru-Rong Ji教授为通迅作者。

左1为徐劲,左8为Ru-Rong Ji教授


财经自媒体联盟

4000520066 欢迎批评指正
All Rights Reserved 新浪公司 版权所有















































 第一财经日报
第一财经日报  每日经济新闻
每日经济新闻  贝壳财经视频
贝壳财经视频  尺度商业
尺度商业  财联社APP
财联社APP  量子位
量子位  财经网
财经网  华商韬略
华商韬略